锌焙砂中,锌及其他金属元素大部分以氧化物形态存在,少部分以铁酸盐、硅酸盐形态存在,在浸出时氧化物可能发生下列反应,生成相应的硫酸盐。
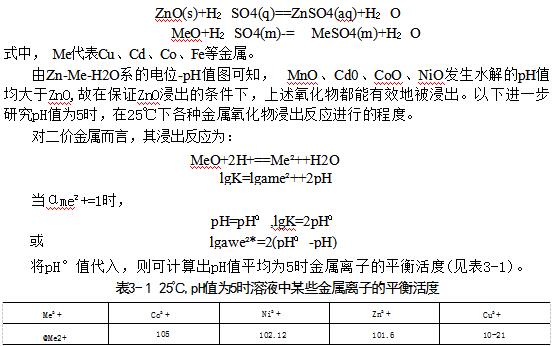
从表3-1可知,在pH值为5时,Co、Ni、Zn的氧化物实际上能完全被浸出,而 Cu²+的活度可达10-2.1,故Cu²+的平衡质量浓度将超过0.5g/L。
中性浸出时,焙烧矿中各组分在浸出时的行为如下:
(1)ZnO 、NiO 、CoO 、CuO 、CdO等,它们与硫酸作用生成MeSO4进入溶液。
(2)Fe203、As203、Sb2O3等,它们与硫酸作用生成Me2(SO4)3进入溶液,然后通 过水解大部分进入浸出渣。
(3)PbO 、Ca0 、MgO 、BaO,PbSO4不入溶液, CaSO4少量入溶液, MgSO4 、BaSO4 部分入溶液,虽这部分物质不进入溶液而绝大部分入渣,但它们消耗了硫酸,因此,不希 望精矿中含量过高。
(4)ZnS 、Fe3O4 、Si02 、MeS 、Au 、Ag等,它们不与硫酸作用而入渣。
(5)Ga、In、Ge、Tl等,在热酸浸出时入溶液,在中性浸出时入渣。
(6)MeO 、Si02 、As20s 、Sb₂Os结合态的SiO2等,在浸出时以硅胶(H2SiO3)进入 溶液,通过水解大部分进入渣中,影响溶液的澄清与分离。砷、锑五氧化物以正酸盐 (如As043-)溶入溶液,然后通过水解进入渣中。
由以上讨论分析可知,浸出后将得到下列物质:
溶液以ZnSO4为主,含有溶解金属Ni、Co、Cu、Cd及少量的Fe、As、Sb和硅胶。
渣以脉石为主,含有不溶金属。
含杂质较多的浸出液不能直接送去电解,需要进行多段净化,在浸出过程中通过控制 适当的终点pH值进行水解,可除去Fe、As、Sb、Si等杂质。
影响浸出速度的因素有以下方面:温度、矿浆搅拌速度、硫酸浓度、焙烧矿的性质、 矿浆黏度。
高温高酸浸出时,铁酸锌的溶解条件为:温度85~95℃,酸度20~60g/L,此时锌的浸出率达95%上下,但溶液含Fe>30g/L。
综上所述,在中性浸出阶段,若最终pH值控制在5左右,锌、钴、镍、镁等均可生 成硫酸盐进入溶液,铅、钙的氧化物也可变成相应的硫酸盐,但PbSO4、CaSO4的溶解度 较小,在25℃时分别为3.9×10²g/L和1.93g/L,因此PbSO4主要进入渣相,CaSO4则部 分溶解入浸出液。In203、Fe3O4、Ga203、SnO2等氧化物由于pH°值很小,主要进入渣, 银也主要进入渣相。
|



